¿Dónde se Encuentra la Masa de un Átomo? Descubre su Ubicación y Significado
La masa de un átomo es un concepto fundamental en la química y la física que nos ayuda a entender la naturaleza de la materia que nos rodea. Pero, ¿alguna vez te has preguntado dónde se encuentra realmente esa masa? En este artículo, vamos a desglosar el tema de la masa atómica, su ubicación dentro del átomo y su significado en diferentes contextos. A medida que profundicemos, exploraremos la estructura del átomo, los componentes que aportan masa, y cómo esta información es crucial para diversas aplicaciones en la ciencia y la tecnología. Si estás listo para sumergirte en el fascinante mundo de la física atómica, sigue leyendo para descubrir todo lo que necesitas saber sobre la masa de un átomo.
La Estructura del Átomo: Un Vistazo General
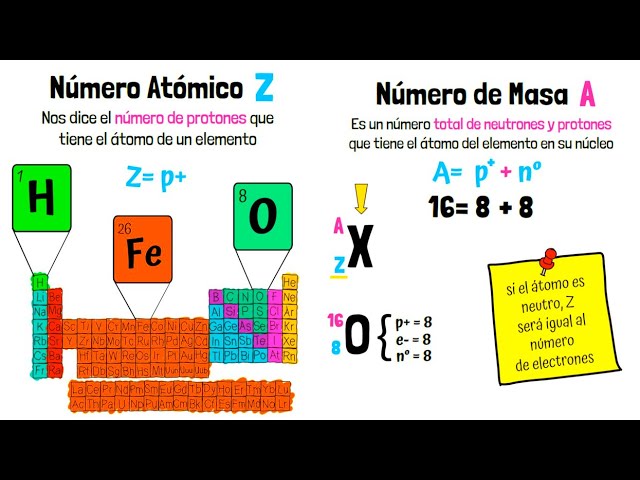
Para entender dónde se encuentra la masa de un átomo, primero debemos conocer su estructura básica. El átomo está compuesto por tres partículas subatómicas principales: protones, neutrones y electrones. Mientras que los electrones orbitan alrededor del núcleo atómico, los protones y neutrones se encuentran en el núcleo. Este núcleo es donde reside la mayor parte de la masa del átomo.
1 Protonas y Neutrones: Los Portadores de Masa
Los protones son partículas con carga positiva que se encuentran en el núcleo. Cada protón tiene una masa aproximada de 1.67 x 10-27 kg. Por otro lado, los neutrones son partículas sin carga, también ubicadas en el núcleo, y tienen una masa similar a la de los protones. En conjunto, los protones y neutrones son responsables de casi toda la masa del átomo, mientras que los electrones, que tienen una masa mucho menor (aproximadamente 1/1836 de la masa de un protón), contribuyen muy poco a la masa total.
2 Electrones: Contribución a la Masa Total
A pesar de su insignificante masa, los electrones son esenciales para las propiedades químicas de los átomos. Estos se encuentran en diferentes niveles de energía alrededor del núcleo y determinan cómo interactúa un átomo con otros. Aunque la masa de los electrones no afecta significativamente la masa total del átomo, su distribución y comportamiento son fundamentales para entender la química y la reactividad.
La Masa Atómica: Definición y Cálculo
La masa atómica es la medida que se utiliza para expresar la masa de un átomo en unidades de masa atómica (uma). Esta unidad es útil porque permite comparar la masa de diferentes átomos de manera efectiva. La masa atómica se calcula sumando la masa de los protones y neutrones en el núcleo, dado que son los que aportan la mayor parte de la masa del átomo.
1 Cómo se Calcula la Masa Atómica
La masa atómica se calcula utilizando la siguiente fórmula:
- Masa Atómica = (Número de Protones x Masa de un Protón) + (Número de Neutrones x Masa de un Neutrón)
Por ejemplo, el carbono tiene 6 protones y 6 neutrones, por lo que su masa atómica sería aproximadamente 12 uma. Es importante tener en cuenta que la masa atómica que se encuentra en la tabla periódica es un promedio ponderado de las masas de los isótopos naturales del elemento.
2 Isótopos y su Impacto en la Masa Atómica
Los isótopos son variantes de un mismo elemento que tienen el mismo número de protones pero diferente número de neutrones. Esto significa que los isótopos de un elemento pueden tener diferentes masas atómicas. Por ejemplo, el carbono-12 (con 6 neutrones) y el carbono-14 (con 8 neutrones) son isótopos del carbono. Esta variación en la masa es importante en aplicaciones como la datación por carbono, donde se utiliza el carbono-14 para estimar la edad de restos orgánicos.
La Relación entre Masa y Energía
Un concepto fascinante que surge al estudiar la masa de un átomo es la relación entre masa y energía, tal como se describe en la famosa ecuación de Einstein, E=mc2. Esta ecuación establece que la masa puede ser convertida en energía y viceversa. Esto tiene implicaciones profundas en la física nuclear y en la comprensión de procesos como la fusión y fisión nuclear.
1 Fusión Nuclear: Un Ejemplo de Conversión de Masa a Energía
En la fusión nuclear, dos núcleos atómicos ligeros se combinan para formar un núcleo más pesado, liberando una gran cantidad de energía en el proceso. Este es el mismo proceso que alimenta a las estrellas, incluido nuestro Sol. La masa del núcleo resultante es menor que la suma de las masas de los núcleos originales, y esta «masa perdida» se convierte en energía. Esto es lo que permite que la fusión nuclear sea una fuente de energía tan poderosa.
2 Fisión Nuclear: Descomposición de Masa en Energía
La fisión nuclear, por otro lado, implica la división de un núcleo pesado en núcleos más ligeros, también liberando energía. Este proceso es utilizado en reactores nucleares y armas nucleares. Al igual que en la fusión, la masa de los productos de fisión es menor que la masa del núcleo original, y la diferencia se libera como energía. Esta relación entre masa y energía es fundamental para comprender no solo la física nuclear, sino también el funcionamiento del universo.
La Importancia de la Masa Atómica en la Química
La masa atómica no solo es un concepto teórico; tiene aplicaciones prácticas en el campo de la química. La comprensión de la masa de los átomos es esencial para realizar cálculos estequiométricos, que son necesarios para predecir cómo reaccionan los compuestos químicos entre sí.
1 Cálculos Estequiométricos: La Base de la Química
En las reacciones químicas, los reactivos se combinan en proporciones específicas, y conocer la masa atómica de cada elemento permite a los químicos calcular cuántos gramos de un reactivo se necesitan para reaccionar con otro. Por ejemplo, si sabemos que la masa atómica del oxígeno es 16 uma y la del hidrógeno es 1 uma, podemos calcular que para formar agua (H2O), se necesitan 2 gramos de hidrógeno por cada 16 gramos de oxígeno.
2 La Masa Atómica en la Medicina y Biología
Además de su relevancia en la química, la masa atómica también juega un papel crucial en la medicina y la biología. Por ejemplo, en la tomografía por emisión de positrones (PET), se utilizan isótopos radiactivos que tienen masas atómicas específicas para diagnosticar enfermedades. Estos isótopos emiten radiación que puede ser detectada y utilizada para visualizar procesos biológicos en el cuerpo humano.
La Masa de un Átomo en el Contexto del Modelo Atómico
Con el tiempo, los modelos atómicos han evolucionado para describir mejor la naturaleza del átomo. Desde el modelo de Dalton hasta el modelo cuántico actual, cada uno ha aportado nuevas perspectivas sobre la masa y la estructura atómica.
1 El Modelo de Bohr y la Masa Atómica
El modelo de Bohr, desarrollado a principios del siglo XX, introdujo la idea de que los electrones orbitan el núcleo en niveles de energía discretos. Aunque este modelo fue revolucionario, no tenía en cuenta la masa de los electrones en sus cálculos. Sin embargo, ayudó a establecer la base para el desarrollo posterior de la teoría cuántica.
2 La Mecánica Cuántica y la Masa Atómica
La mecánica cuántica, que surgió en la primera mitad del siglo XX, proporcionó una comprensión más profunda de la masa atómica y la distribución de electrones. Este enfoque reconoce que los electrones no tienen trayectorias definidas, sino que existen en nubes de probabilidad alrededor del núcleo. Este modelo cuántico es fundamental para entender la química moderna y cómo la masa atómica afecta las propiedades de los elementos.
Aplicaciones Prácticas de la Masa Atómica
La comprensión de la masa atómica y su ubicación en el átomo tiene múltiples aplicaciones en diversas disciplinas. Desde la química hasta la física nuclear, la masa atómica es un concepto esencial que permite a los científicos y profesionales aplicar sus conocimientos en situaciones prácticas.
1 En la Industria Química
En la industria química, la masa atómica es fundamental para la producción de compuestos. Los químicos utilizan esta información para diseñar procesos de síntesis eficientes y seguros. Por ejemplo, al producir fertilizantes, se deben conocer las proporciones exactas de nitrógeno, fósforo y potasio, que dependen de las masas atómicas de estos elementos.
2 En la Investigación Científica
La investigación en física y química a menudo se basa en la medición precisa de la masa atómica. Los avances en técnicas de espectrometría de masas han permitido a los científicos identificar isótopos y estudiar reacciones químicas con un nivel de precisión sin precedentes. Esto ha llevado a descubrimientos significativos en campos como la biología molecular y la medicina.
La masa de un átomo se encuentra principalmente en su núcleo, compuesto por protones y neutrones. Esta masa es crucial no solo para entender la estructura atómica, sino también para aplicar este conocimiento en diversas áreas de la ciencia y la tecnología. La relación entre masa y energía, así como la importancia de la masa atómica en reacciones químicas y aplicaciones prácticas, demuestra que la masa de un átomo es un tema de gran relevancia en nuestro mundo.
FAQ (Preguntas Frecuentes)
¿Qué es la masa atómica y cómo se mide?
La masa atómica es la medida de la masa de un átomo, generalmente expresada en unidades de masa atómica (uma). Se mide sumando la masa de los protones y neutrones en el núcleo. La masa de los electrones es tan pequeña que se ignora en la mayoría de los cálculos. Por ejemplo, el carbono tiene una masa atómica de aproximadamente 12 uma.
¿Por qué la masa de los electrones es tan pequeña?
Los electrones son partículas subatómicas con una masa mucho menor que la de los protones y neutrones. Su masa es aproximadamente 1/1836 de la masa de un protón. Aunque su contribución a la masa total del átomo es mínima, son fundamentales para las propiedades químicas y la formación de enlaces entre átomos.
¿Qué son los isótopos y cómo afectan la masa atómica?
Los isótopos son variantes de un elemento que tienen el mismo número de protones pero diferente número de neutrones. Esto significa que tienen diferentes masas atómicas. Por ejemplo, el carbono-12 y el carbono-14 son isótopos del carbono. La existencia de isótopos es importante en aplicaciones como la datación por carbono y en medicina.
¿Cómo se relaciona la masa atómica con la energía nuclear?
La masa atómica está estrechamente relacionada con la energía nuclear a través de la ecuación de Einstein, E=mc2. En procesos como la fusión y fisión nuclear, una pequeña cantidad de masa se convierte en una gran cantidad de energía. Esto es fundamental para entender cómo funcionan las reacciones nucleares y sus aplicaciones en energía y medicina.
¿Por qué es importante conocer la masa atómica en química?
Conocer la masa atómica es esencial en química para realizar cálculos estequiométricos, que permiten predecir cómo reaccionan los compuestos entre sí. También es importante para entender la reactividad de los elementos y diseñar procesos químicos eficientes en la industria.
¿Cómo ha evolucionado el concepto de masa atómica?
El concepto de masa atómica ha evolucionado desde los modelos atómicos de Dalton y Thomson hasta el modelo cuántico actual. Cada avance ha proporcionado una comprensión más profunda de la estructura atómica y la masa, permitiendo aplicaciones más precisas en la química y la física moderna.
¿Qué aplicaciones tiene la masa atómica en la vida cotidiana?
La masa atómica tiene múltiples aplicaciones en la vida cotidiana, desde la producción de alimentos y productos químicos hasta la medicina y la tecnología. Por ejemplo, en la industria farmacéutica, la masa atómica es crucial para formular medicamentos efectivos y seguros.






