Diferencia entre Masa Atómica y Número Atómico: Guía Completa para Entender la Química
# Diferencia entre Masa Atómica y Número Atómico: Guía Completa para Entender la Química
La química es una de las ciencias más fascinantes, y entender sus conceptos básicos es esencial para cualquier persona interesada en el mundo que nos rodea. Dos términos que a menudo generan confusión son «masa atómica» y «número atómico». Aunque ambos conceptos están relacionados con los elementos químicos, cada uno tiene un significado y una función específica. ¿Te has preguntado alguna vez por qué es importante diferenciar entre estos dos términos? En esta guía completa, exploraremos la diferencia entre masa atómica y número atómico, su relevancia en la química y cómo se utilizan en diversas aplicaciones. Te prometemos que al finalizar este artículo, tendrás una comprensión clara y profunda de estos conceptos fundamentales.
## ¿Qué es el Número Atómico?
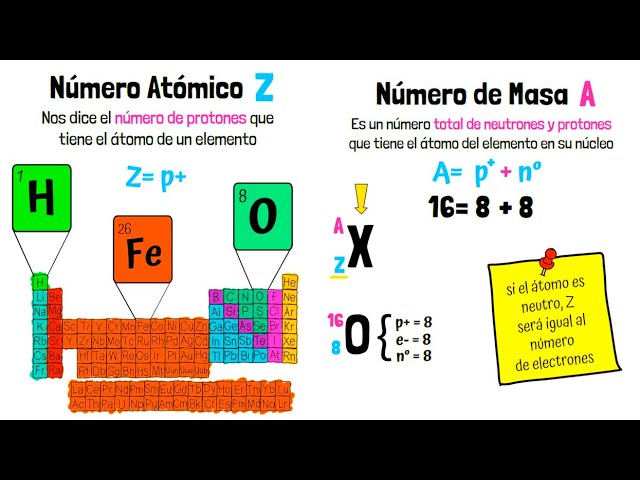
El número atómico es una de las propiedades más importantes de un elemento químico. Se define como el número de protones que se encuentran en el núcleo de un átomo. Este número no solo identifica al elemento, sino que también determina su posición en la tabla periódica.
### Importancia del Número Atómico
1. Identificación de Elementos: Cada elemento tiene un número atómico único. Por ejemplo, el hidrógeno tiene un número atómico de 1, mientras que el carbono tiene un número atómico de 6. Esta singularidad permite clasificar y organizar los elementos de manera efectiva.
2. Propiedades Químicas: El número atómico influye en las propiedades químicas del elemento. Los elementos con el mismo número atómico suelen tener comportamientos similares en reacciones químicas.
3. Cálculo de Cargas: El número atómico también es crucial para entender la carga de los átomos. En un átomo neutro, el número de electrones es igual al número de protones, lo que significa que el número atómico también indica la carga positiva total del núcleo.
### Ejemplo Práctico
Imagina que estás estudiando el oxígeno, que tiene un número atómico de 8. Esto significa que en su núcleo hay 8 protones. Como el oxígeno es un elemento esencial para la vida, entender su número atómico es fundamental para comprender su papel en procesos biológicos como la respiración.
## ¿Qué es la Masa Atómica?
La masa atómica, por otro lado, se refiere a la masa promedio de un átomo de un elemento en unidades de masa atómica (uma o amu). Esta masa se calcula considerando la abundancia de los isótopos del elemento en la naturaleza y sus respectivas masas.
### Importancia de la Masa Atómica
1. Cálculos Químicos: La masa atómica es fundamental en las reacciones químicas, ya que se utiliza para calcular las cantidades de reactivos y productos. Conocer la masa atómica de un elemento te permite determinar cuántos átomos se necesitan para una reacción específica.
2. Comparaciones entre Elementos: La masa atómica permite comparar elementos entre sí. Por ejemplo, el carbono tiene una masa atómica de aproximadamente 12, mientras que el oxígeno tiene una masa atómica de aproximadamente 16. Esto puede influir en la forma en que se combinan en compuestos.
3. Entendimiento de Isótopos: La masa atómica también se relaciona con los isótopos. Por ejemplo, el carbono tiene isótopos como el carbono-12 y el carbono-14. La masa atómica promedio refleja la abundancia de estos isótopos en la naturaleza.
### Ejemplo Práctico
Considera el cloro, que tiene una masa atómica de aproximadamente 35.5 uma. Esto indica que en promedio, un átomo de cloro pesa 35.5 veces más que un átomo de hidrógeno. Este dato es crucial cuando se realizan cálculos en reacciones químicas que involucran cloro.
## Diferencias Clave entre Masa Atómica y Número Atómico
Para entender la diferencia entre masa atómica y número atómico, es útil resumir sus características principales:
1. Definición:
– Número Atómico: Número de protones en el núcleo de un átomo.
– Masa Atómica: Masa promedio de un átomo de un elemento, considerando la abundancia de sus isótopos.
2. Ubicación en la Tabla Periódica:
– Número Atómico: Determina la posición del elemento en la tabla periódica.
– Masa Atómica: Se encuentra en la parte inferior del símbolo del elemento en la tabla periódica.
3. Función:
– Número Atómico: Identifica el elemento y sus propiedades químicas.
– Masa Atómica: Se utiliza para cálculos en reacciones químicas y comparaciones entre elementos.
## Relación entre Masa Atómica y Número Atómico
Aunque masa atómica y número atómico son conceptos diferentes, están interrelacionados. El número atómico determina la identidad de un elemento, mientras que la masa atómica proporciona información sobre su estructura y comportamiento en reacciones químicas.
### Ejemplo de Interrelación
Tomemos el ejemplo del carbono. Su número atómico es 6, lo que significa que tiene 6 protones. La masa atómica promedio del carbono es 12.01 uma, lo que refleja la presencia de isótopos como el carbono-12 y el carbono-14. Esta relación es esencial para comprender cómo el carbono interactúa en diversas reacciones químicas, como la fotosíntesis o la formación de compuestos orgánicos.
## Aplicaciones Prácticas en Química
La comprensión de la diferencia entre masa atómica y número atómico tiene aplicaciones prácticas en diversas áreas de la química y la ciencia en general.
1. Química Analítica: En la química analítica, la masa atómica se utiliza para calcular concentraciones y preparar soluciones. Por ejemplo, al preparar una solución de cloruro de sodio (NaCl), conocer la masa atómica del sodio y del cloro es fundamental para determinar la cantidad necesaria.
2. Biología Molecular: En biología molecular, la masa atómica y el número atómico son esenciales para comprender la estructura de biomoléculas como proteínas y ácidos nucleicos. La composición atómica de estas moléculas afecta su función biológica.
3. Nuclear y Energía: En el campo de la energía nuclear, el número atómico es crucial para identificar elementos radiactivos, mientras que la masa atómica se utiliza para calcular la energía liberada en reacciones nucleares.
## Preguntas Frecuentes (FAQ)
### 1. ¿Cuál es la diferencia entre isótopos y número atómico?
Los isótopos son átomos del mismo elemento que tienen el mismo número atómico pero diferente masa atómica debido a la variación en el número de neutrones. Por ejemplo, el carbono-12 y el carbono-14 son isótopos del carbono, ambos con un número atómico de 6, pero con masas atómicas diferentes.
### 2. ¿Por qué la masa atómica no es un número entero?
La masa atómica no es un número entero porque representa un promedio ponderado de las masas de todos los isótopos de un elemento en función de su abundancia en la naturaleza. Esto significa que los elementos con múltiples isótopos tendrán masas atómicas que pueden ser fraccionarias.
### 3. ¿Cómo se calcula la masa atómica de un elemento?
La masa atómica se calcula sumando las masas de los isótopos multiplicadas por su abundancia relativa. Por ejemplo, si un elemento tiene dos isótopos, se multiplica la masa de cada isótopo por su porcentaje de abundancia y se suman los resultados para obtener la masa atómica promedio.
### 4. ¿El número atómico puede cambiar?
El número atómico de un elemento es constante y no cambia, ya que define la identidad del elemento. Sin embargo, los átomos de un elemento pueden existir en diferentes estados (iones) donde pueden ganar o perder electrones, pero su número de protones, y por lo tanto su número atómico, permanece igual.
### 5. ¿Cómo afecta el número atómico a las propiedades químicas de un elemento?
El número atómico determina la configuración electrónica del átomo, lo que a su vez afecta cómo el elemento interactúa con otros elementos. Elementos con el mismo número atómico tienden a tener propiedades químicas similares, lo que facilita su clasificación en grupos en la tabla periódica.
### 6. ¿Qué papel juegan la masa atómica y el número atómico en la formación de compuestos?
La masa atómica y el número atómico son fundamentales para entender cómo los elementos se combinan para formar compuestos. La masa atómica se utiliza para calcular las proporciones en las que los elementos se combinan, mientras que el número atómico ayuda a predecir las propiedades del compuesto resultante.
### 7. ¿Por qué es importante la masa atómica en la medicina?
La masa atómica es crucial en la medicina, especialmente en el desarrollo de tratamientos y diagnósticos. Por ejemplo, en la terapia con isótopos radiactivos, conocer la masa atómica de los isótopos utilizados permite calcular dosis y prever efectos en el organismo.






