Enunciado de la Ley de Conservación de la Masa: Principios y Aplicaciones
Enunciado de la Ley de Conservación de la Masa: Principios y Aplicaciones
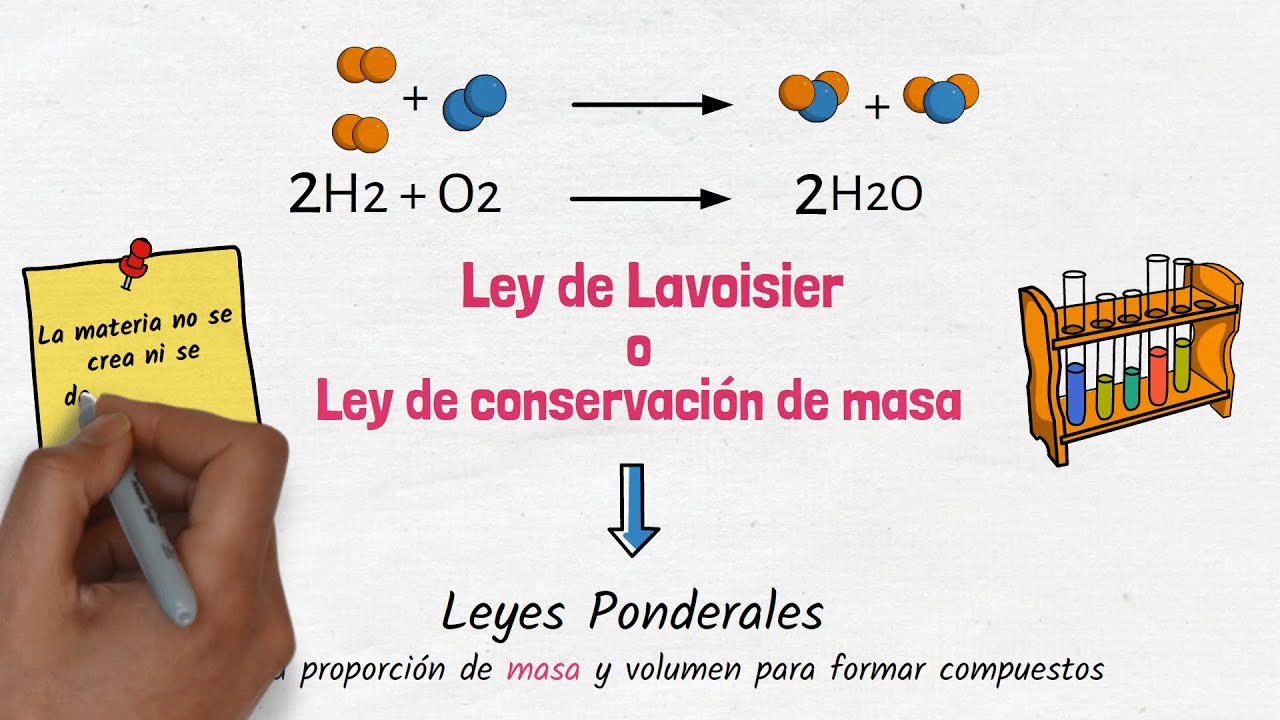
La Ley de Conservación de la Masa es uno de los pilares fundamentales de la química y la física, con implicaciones que van más allá de los laboratorios y las aulas. Este principio, enunciado por Antoine Lavoisier en el siglo XVIII, establece que en una reacción química, la masa total de los reactivos es igual a la masa total de los productos. Esto significa que la materia no se crea ni se destruye, sino que simplemente se transforma. La relevancia de esta ley es inmensa, ya que nos permite entender procesos químicos y físicos, así como aplicar este conocimiento en diversas disciplinas, desde la ingeniería hasta la biología.
En este artículo, exploraremos en detalle el enunciado de la Ley de Conservación de la Masa, sus principios fundamentales y sus aplicaciones prácticas en diferentes campos. Desde la química básica hasta la sostenibilidad ambiental, descubrirás cómo este concepto se manifiesta en nuestra vida cotidiana y cómo influye en el desarrollo de tecnologías modernas. Acompáñanos en este recorrido por la materia y su inmutable esencia.
1. Historia y Origen de la Ley de Conservación de la Masa
La historia de la Ley de Conservación de la Masa comienza en el siglo XVIII con Antoine Lavoisier, considerado el «padre de la química moderna». Su trabajo fue fundamental para establecer la base científica de la química y, a través de una serie de experimentos meticulosos, Lavoisier llegó a la conclusión de que la masa se conserva en las reacciones químicas.
1.1. Experimentos de Lavoisier
Lavoisier realizó experimentos que involucraban la combustión de sustancias en un recipiente cerrado. Mediante pesajes precisos antes y después de las reacciones, demostró que la masa de los reactivos siempre coincidía con la masa de los productos formados. Por ejemplo, al quemar fósforo en un frasco cerrado, Lavoisier observó que el peso total del frasco no cambiaba, a pesar de que el fósforo se transformaba en un nuevo compuesto.
1.2. Implicaciones Filosóficas y Científicas
La Ley de Conservación de la Masa no solo tuvo un impacto en la química, sino que también desafió ideas previas sobre la naturaleza de la materia. Antes de Lavoisier, muchos creían que la materia podía ser creada o destruida. La demostración de que la masa es constante en reacciones químicas sentó las bases para el desarrollo de la teoría atómica y ayudó a establecer la química como una ciencia cuantitativa.
2. Principios Fundamentales de la Ley de Conservación de la Masa
La Ley de Conservación de la Masa se basa en varios principios que son cruciales para su comprensión. Estos principios no solo son aplicables en química, sino que también se extienden a otras ciencias naturales.
2.1. La Materia es Inmutable
Una de las ideas clave detrás de esta ley es que la materia no se crea ni se destruye. En cualquier reacción química, aunque los enlaces entre los átomos se rompen y se forman nuevos, el número total de átomos permanece constante. Esto significa que los elementos que participan en una reacción se reorganizan, pero no desaparecen.
2.2. Reacciones Químicas y Masa
En una reacción química típica, los reactivos se transforman en productos. La masa de los reactivos, sumada antes de la reacción, es igual a la masa de los productos obtenidos. Por ejemplo, si mezclamos 2 gramos de hidrógeno con 16 gramos de oxígeno, obtendremos 18 gramos de agua. Este principio se aplica a todas las reacciones químicas, desde las más simples hasta las más complejas.
2.3. Aplicaciones en la Ciencia y la Tecnología
El entendimiento de la Ley de Conservación de la Masa es esencial en campos como la ingeniería química, la biología y la física. En ingeniería química, por ejemplo, se utiliza para diseñar procesos industriales eficientes. En biología, ayuda a comprender el metabolismo y las reacciones bioquímicas en los organismos vivos.
3. Aplicaciones Prácticas en la Industria
La Ley de Conservación de la Masa tiene múltiples aplicaciones en la industria, desde la producción de alimentos hasta la manufactura de productos químicos. Estos principios son esenciales para garantizar la eficiencia y la sostenibilidad en los procesos industriales.
3.1. Procesos Químicos en la Industria
En la industria química, los ingenieros utilizan la Ley de Conservación de la Masa para calcular las cantidades de reactivos necesarios y prever la cantidad de productos que se generarán. Por ejemplo, en la producción de amoníaco a partir de nitrógeno e hidrógeno, los ingenieros deben asegurarse de que las proporciones de entrada y salida se ajusten a la ley, optimizando así el proceso y minimizando el desperdicio.
3.2. Producción de Alimentos
En la industria alimentaria, la conservación de la masa es vital para asegurar la calidad y la seguridad de los productos. Los procesos de cocción, fermentación y conservación deben tener en cuenta la masa de los ingredientes para garantizar que se mantenga la proporción adecuada de nutrientes y sabor. Por ejemplo, al hacer pan, es crucial medir correctamente la harina, el agua y la levadura para obtener un producto final que cumpla con los estándares deseados.
3.3. Sostenibilidad y Medio Ambiente
La Ley de Conservación de la Masa también juega un papel crucial en la sostenibilidad ambiental. Al comprender cómo se transforma la materia en diferentes procesos, es posible diseñar sistemas que reduzcan el desperdicio y promuevan el reciclaje. Por ejemplo, en el tratamiento de residuos, los ingenieros utilizan estos principios para maximizar la recuperación de materiales y minimizar el impacto ambiental de los desechos.
4. La Ley de Conservación de la Masa en la Biología
La biología también se beneficia enormemente de la Ley de Conservación de la Masa, especialmente en el estudio de procesos metabólicos y en la comprensión de cómo los organismos obtienen y utilizan la materia.
4.1. Metabolismo Celular
El metabolismo es el conjunto de reacciones químicas que ocurren dentro de las células. La Ley de Conservación de la Masa se aplica aquí al analizar cómo los nutrientes se convierten en energía y cómo los desechos se eliminan. Por ejemplo, en la respiración celular, los organismos convierten glucosa y oxígeno en dióxido de carbono y agua, conservando la masa total de los reactivos y productos.
4.2. Ciclos Biogeoquímicos
Los ciclos biogeoquímicos, como el ciclo del carbono y el ciclo del nitrógeno, son ejemplos de cómo la Ley de Conservación de la Masa se manifiesta en la naturaleza. En estos ciclos, los elementos se mueven entre los organismos y el medio ambiente, pero la cantidad total de cada elemento permanece constante. Esto es crucial para el equilibrio ecológico y la salud del planeta.
4.3. Aplicaciones Médicas
En el campo de la medicina, la Ley de Conservación de la Masa se aplica en diversas áreas, como la farmacología y la toxicología. Por ejemplo, al desarrollar medicamentos, es esencial entender cómo se metabolizan en el cuerpo y cómo se distribuyen y eliminan. Esto permite a los médicos calcular las dosis adecuadas y prever interacciones entre diferentes sustancias.
5. Retos y Consideraciones en la Aplicación de la Ley de Conservación de la Masa
A pesar de su importancia, la aplicación de la Ley de Conservación de la Masa no está exenta de desafíos. En ciertas condiciones, como en reacciones nucleares, la masa puede no parecer conservarse debido a la conversión de masa en energía, según la famosa ecuación de Einstein, E=mc².
5.1. Reacciones Nucleares
En reacciones nucleares, como la fisión y la fusión, la masa total de los reactivos puede ser diferente de la masa de los productos. Esto se debe a que parte de la masa se convierte en energía. Por lo tanto, aunque la Ley de Conservación de la Masa se aplica a reacciones químicas, es importante considerar la Ley de Conservación de la Energía en estos casos.
5.2. Mediciones y Errores Experimentales
La precisión en las mediciones es crucial para aplicar correctamente la Ley de Conservación de la Masa. En experimentos, los errores en la pesaje o en la manipulación de reactivos pueden llevar a resultados incorrectos. Por ello, es fundamental utilizar equipos de medición precisos y seguir protocolos estrictos en los laboratorios.
5.3. Complejidad de Reacciones Químicas
Algunas reacciones químicas son complejas y pueden involucrar múltiples pasos. En estos casos, la conservación de la masa debe analizarse en cada etapa del proceso. Esto requiere un conocimiento profundo de la química involucrada y puede complicar la predicción de resultados.
6. Preguntas Frecuentes (FAQ)
¿Qué es la Ley de Conservación de la Masa?
La Ley de Conservación de la Masa establece que en una reacción química, la masa total de los reactivos es igual a la masa total de los productos. Esto significa que la materia no se crea ni se destruye, sino que se transforma de una forma a otra. Este principio es fundamental en química y tiene aplicaciones en diversas disciplinas.
¿Quién formuló la Ley de Conservación de la Masa?
Antoine Lavoisier, un químico francés del siglo XVIII, es el científico que formuló la Ley de Conservación de la Masa. A través de experimentos cuidadosos, demostró que la masa de los reactivos en una reacción química siempre coincide con la masa de los productos generados.
¿Cuáles son las aplicaciones de la Ley de Conservación de la Masa en la industria?
La Ley de Conservación de la Masa se aplica en diversas industrias, como la química y la alimentaria. Permite a los ingenieros calcular las cantidades necesarias de reactivos, optimizar procesos de producción y garantizar la calidad de los productos. También es fundamental en el diseño de procesos sostenibles que minimizan el desperdicio.
¿Cómo se aplica la Ley de Conservación de la Masa en la biología?
En biología, la Ley de Conservación de la Masa se aplica al metabolismo celular y a los ciclos biogeoquímicos. Por ejemplo, en la respiración celular, los nutrientes se transforman en energía, conservando la masa total. También es relevante en la comprensión de cómo los elementos se mueven entre los organismos y el medio ambiente.
¿Existen excepciones a la Ley de Conservación de la Masa?
Sí, hay excepciones en reacciones nucleares, donde la masa puede no parecer conservarse debido a la conversión de masa en energía. En estos casos, se debe considerar la Ley de Conservación de la Energía, que establece que la energía total en un sistema cerrado se conserva.
¿Por qué es importante la Ley de Conservación de la Masa en la sostenibilidad ambiental?
La Ley de Conservación de la Masa es crucial para la sostenibilidad ambiental, ya que permite diseñar procesos que minimizan el desperdicio y promueven el reciclaje. Comprender cómo se transforma la materia en diferentes procesos ayuda a desarrollar tecnologías más limpias y eficientes, contribuyendo a la protección del medio ambiente.
¿Cómo se mide la masa en experimentos químicos?
La masa en experimentos químicos se mide utilizando balanzas precisas que permiten obtener resultados exactos. Es fundamental seguir protocolos de laboratorio rigurosos y asegurar que los reactivos estén bien pesados para aplicar correctamente la Ley de Conservación de la Masa en los experimentos.






